-
電子遞交的合規(guī)性與風(fēng)險(xiǎn)管理 歐盟要求申請(qǐng)人確保電子資料與紙質(zhì)版本完全一致,若未在規(guī)定時(shí)間提交紙質(zhì)文件可能導(dǎo)致注冊(cè)終止。驗(yàn)證過程中,...了解更多
-
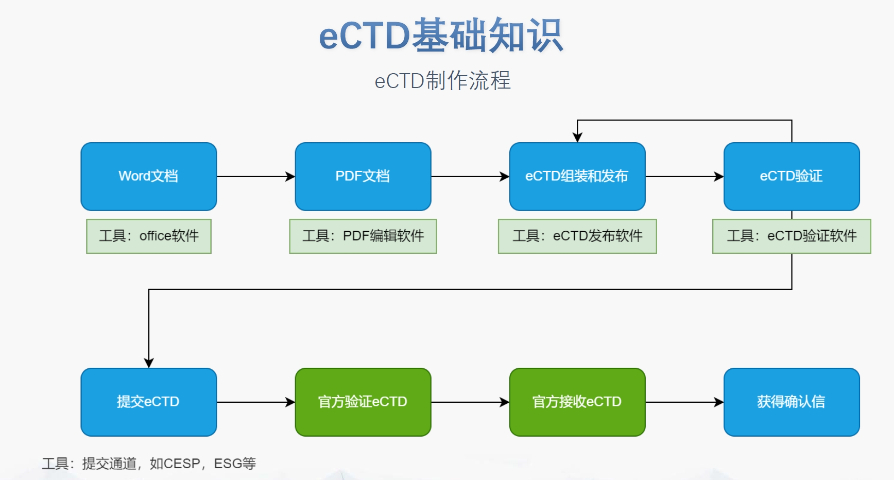
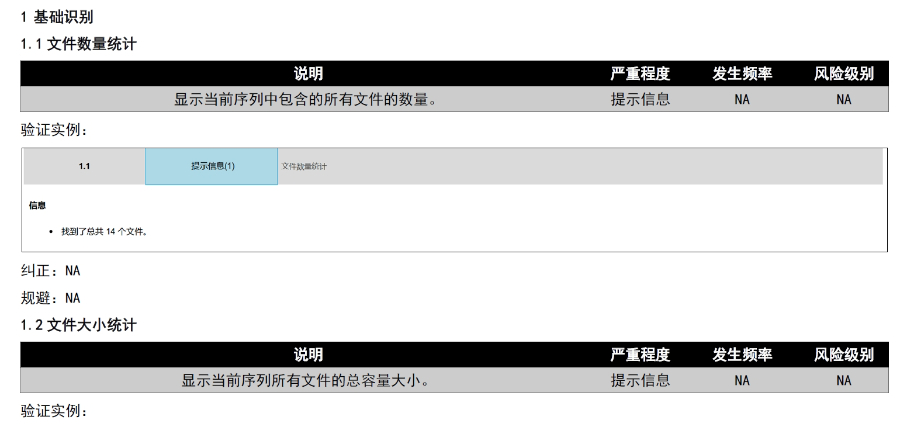
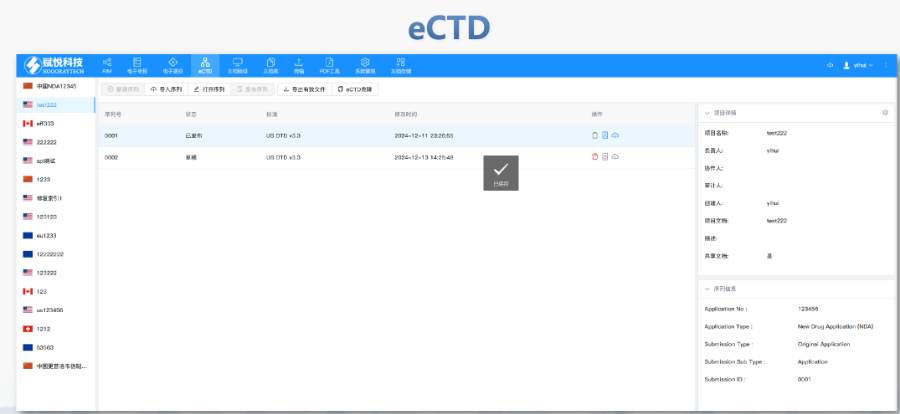
《中國(guó)eCTD驗(yàn)證實(shí)踐手冊(cè)》作為2025年2月發(fā)布的技術(shù)指南(發(fā)布日期見),為藥品注冊(cè)申請(qǐng)人提供了系統(tǒng)化的eCTD申報(bào)驗(yàn)證操作指引...了解更多
-
緊急申報(bào)與特殊通道:FDA設(shè)置緊急申報(bào)通道(如Pre-EUA和EUA),允許在公共衛(wèi)生事件中快速提交資料。此類申請(qǐng)需在模塊1.19...了解更多
-
爭(zhēng)議解決與法律救濟(jì) 若申請(qǐng)人對(duì)審評(píng)結(jié)果有異議,可向EMA的CHMP申請(qǐng)重審查,或在歐盟法院提起行政訴訟。eCTD的完整提交記錄可作...了解更多