商機詳情 -
重慶分子研究高鹽核酸酶70950-160
三種AAV載體的生產體系(三質粒瞬轉體系、桿狀病毒表達載體體系以及包裝細胞體系) 中都會出現三種衣殼:完整衣殼(full capsid)、部分衣殼(partial capsid),和空衣殼(empty capsid)。其中完整衣殼包含正確的DNA序列,是人們所期待的產品;部分衣殼和空衣殼包含部分不包含目的基因,屬于生產中的雜質,約占細胞生產的總AAV顆粒的50%-90%。空衣殼/部分衣殼有如下幾種危害:1), 影響產品的純度,2), 增加終產品的免疫原性,3), 與完整衣殼競爭infection細胞上的載體結合受體,抑制完整衣殼的轉導,4),增加總體病毒載量。部分衣殼與空衣殼地存在嚴重地影響了AAV產品的安全性和有效性,因此監管機構強烈建議在整個生產過程中監控空/完整衣殼比(空殼率)。無錫高鹽核酸酶產品質量哪家好呢,歡迎咨詢上海倍篤生物 。重慶分子研究高鹽核酸酶70950-160

基因療法制造商面臨的挑戰與抗體療法剛出現時單克隆抗體制造商面臨的挑戰相似。例如,在生產、儲存和處理過程中,單克隆抗體也會受到低滴度、產品和工藝相關雜質和降解的挑戰。盡管與重組單克隆抗體相比,單劑量AAV產品與工藝相關雜質相關的風險可能更低(取決于雜質的類型、劑量和給藥途徑),但這也不能忽視。由于這些相似性,制藥商、化學品和輔料供應商有機會進行合作,并開發創新的解決方案,以實現穩健和成本效益高的AAV產品生產。重慶分子研究高鹽核酸酶70950-160上海高鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。
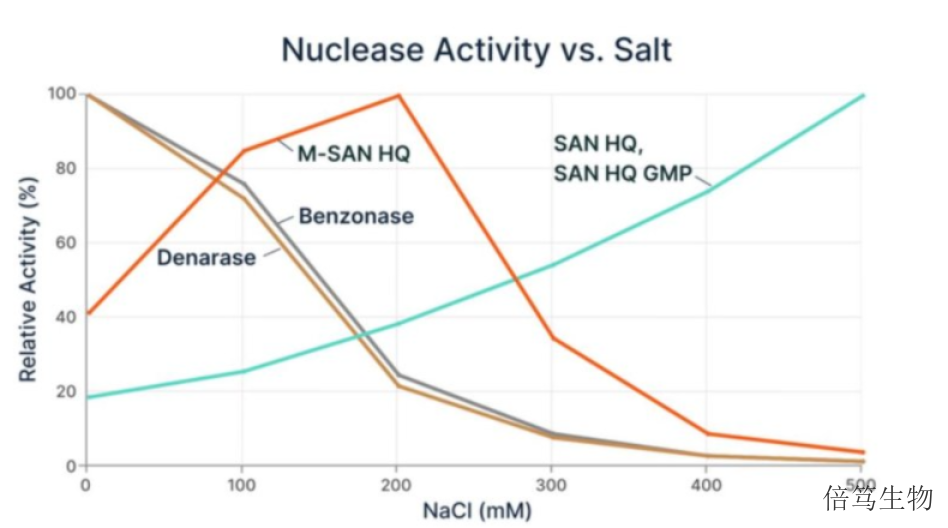
ArcticZymes廠家對鹽活性核酸酶系列產品(Salt Active Nucleases,SANs)的生產及質控,包括SAN HQ高鹽核酸酶和M-SAN HQ中鹽核酸酶,在符合ISO13485:2016體系基礎上,增加了cGMP質控標準,如microbes、endotoxin、蛋白酶等;同時提供TSE/BSE聲明、無動物源(Animal-Origin Free)聲明、非轉基因聲明等文件協助藥物申報。此外,ArcticZymes的生產場地接受客戶的定期審計,其第三方審計文件已得到國際TOP CDMO及Biotech的認可,并已經成為國際TOP CDMO的供應商。具體文件體系可以跟廠家或對應銷售人員聯系。
宿主細胞DNA殘留的擔憂是基于致ai風險理論,特別是生產細胞系所包含的致ai序列,比如較常見腺病毒基因E1A和E1B(HEK293, PerC.6 和CAP 細胞系),人乳tou瘤病毒E6和E7基因(HeLa細胞系)等。當使用致ai細胞系生產AAV時,下游純化須盡可能減少殘留DNA。工業上一般使用核酸酶分解殘留DNA,普遍認為小于200 bp的DNA片段可有效降低致ai風險。宿主細胞蛋白殘留與免疫原性、炎癥或過敏性休克有關。盡管與非人類的生產原料相比(非人類細胞系如BHK21或昆蟲細胞,以及輔助病毒如HSV、腺病毒、桿狀病毒),人類細胞免疫原性比較弱。在符合ISO13485:2016體系基礎上,增加了cGMP相應要求。
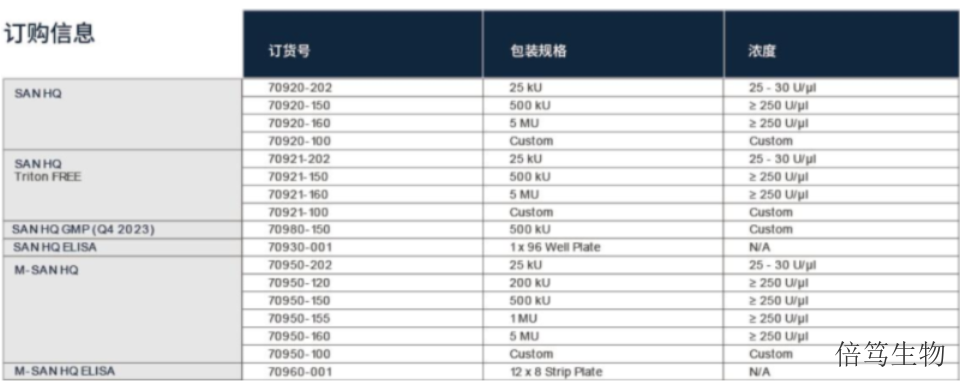
殘留的宿主DNA是生產中產生的雜質,其存在潛在的致瘤性、傳染性和免疫原性等風險。相關研究表明,基因的大小普遍在200bp以上,因此大于200bp有可能會有一定的致病性,而且殘留DNA片段越大,生物制品的風險等級越高。因此,各國監管機構對其提出了嚴格要求。美國食品藥品監督管理局(FDA)在《關于人類基因zhiliao新產品生產指導文件》中明確指出HCD的片段要小于200bp。2022年5月,國家藥品監督管理局藥品評審中心(CDE)發布的《體內基因藥物產品藥學研究與評價技術指導原則(試行)》中也明確指出需對DNA殘留量和殘留片段大小進行控制,建議盡量將DNA殘留片段的大小控制在200bp以下。使用SAN HQ高鹽核酸酶可以更少的酶量獲得更高的去除率,對載體的產量和活性沒有任何負面影響;北京ArcticZymes高鹽核酸酶70921-160
常州高鹽核酸酶售后服務哪家好呢,歡迎咨詢上海倍篤生物 。重慶分子研究高鹽核酸酶70950-160
在生物工藝中,核酸酶的主要作用是高效消化宿主細胞DNA(HCD),并將其分解成足夠小的片段,以便在下游純化過程中去除。雖然大多數核酸酶可以在生理鹽條件下高效地將裸DNA降解成微小片段,比如Benzonase和SANs都可以把dsDNA分解成小于8nt的寡核苷酸鏈,但實際生產中的核酸污染情況更加復雜。HCD通常以染色質形式存在,與細胞裂解碎片、病毒顆粒等結合在一起,影響核酸酶的識別及剪切。因此,HCD去除的關鍵在于——核酸酶如何在復雜的生產體系中識別并剪切HCD。重慶分子研究高鹽核酸酶70950-160