商機(jī)詳情 -
吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
臨床前動(dòng)物實(shí)驗(yàn)的標(biāo)準(zhǔn)操作規(guī)程以及實(shí)驗(yàn)計(jì)劃和實(shí)驗(yàn)方案制定:醫(yī)療器械的安全性評(píng)估通常基于所提供有效科學(xué)證據(jù)的動(dòng)物實(shí)驗(yàn)研究,應(yīng)具有適當(dāng)?shù)臉?biāo)準(zhǔn)操作規(guī)程,以確保數(shù)據(jù)的質(zhì)量和完整性。研究機(jī)構(gòu)應(yīng)當(dāng)制定與其業(yè)務(wù)相適應(yīng)的標(biāo)準(zhǔn)操作規(guī)程。關(guān)于需要制定的標(biāo)準(zhǔn)操作規(guī)程可參考《藥物非臨床研究質(zhì)量管理規(guī)范》第七章的合計(jì)15項(xiàng)條款。建議臨床前動(dòng)物實(shí)驗(yàn)研究包括適當(dāng)?shù)目刂拼胧┮员M量減少實(shí)驗(yàn)的變異性和差錯(cuò)。這樣的措施包括但不限于在試驗(yàn)過(guò)程中盡量減少影響實(shí)驗(yàn)動(dòng)物的因素。生物藥臨床前動(dòng)物實(shí)驗(yàn)外包;吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
藥物在進(jìn)入市場(chǎng)前必須通過(guò)一系列嚴(yán)格的試驗(yàn),其中包括化合物的合成、臨床前動(dòng)物試驗(yàn)和人體臨床試驗(yàn)等。藥物試驗(yàn)的不同階段將分別研究藥物的安全性、有效性、理想的給藥途徑、適宜的使用劑量,以及對(duì)患者生活質(zhì)量的影響等。美國(guó)新藥評(píng)審系統(tǒng)被公認(rèn)為在世界上是**嚴(yán)格的。根據(jù)Tufs藥物發(fā)展研究中心2001年的報(bào)告,平均起來(lái),一種新藥從實(shí)驗(yàn)室合成,篩選開(kāi)始到***被批準(zhǔn)上市,用于患者,共要花費(fèi)大約8億美元,費(fèi)時(shí)10-15年。在被篩選的5000-10000個(gè)化合物中,250個(gè)可以進(jìn)入臨床前試驗(yàn),而其中只有5個(gè)可以進(jìn)入臨床試驗(yàn),**終*有1個(gè)能被批準(zhǔn)上市。福建高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)是什么中成藥臨床前動(dòng)物實(shí)驗(yàn)指導(dǎo)原則;
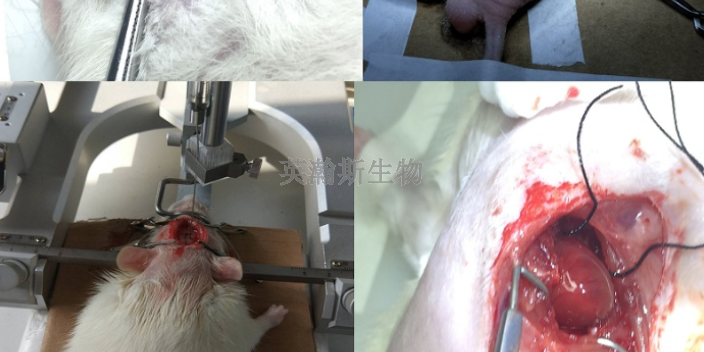
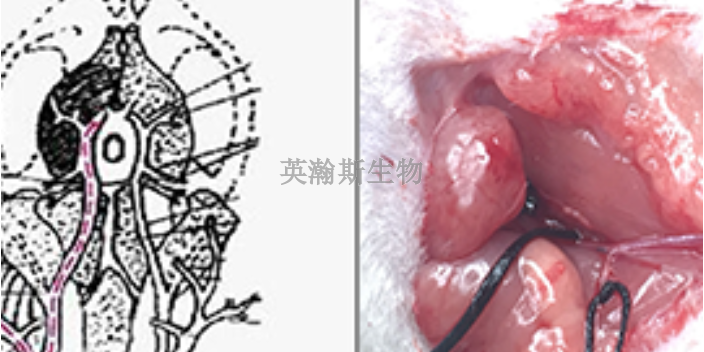
英瀚斯生物專(zhuān)做臨床前動(dòng)物實(shí)驗(yàn)。如果說(shuō)異種移植已處在突破的“前夜”,那么豬胰島移植***Ⅰ型糖尿病已成為實(shí)實(shí)在在的突破“前哨”。這一次,中國(guó)科學(xué)家走在了世界的前列。2002年國(guó)內(nèi)科學(xué)家取得了進(jìn)軍異種移植后的***個(gè)重要突破:豬胰島細(xì)胞經(jīng)肝動(dòng)脈移植***糖尿病在臨床前動(dòng)物試驗(yàn)中首先獲得成功。當(dāng)時(shí),國(guó)際上普遍采用的是將胰島通過(guò)肝臟的門(mén)靜脈植入,但這種方法有時(shí)可能造成肝臟壞死,國(guó)內(nèi)科學(xué)家創(chuàng)立的新方法使得手術(shù)安全性明顯增加。1999年10月,在澳大利亞悉尼舉行的第七屆國(guó)際胰腺胰島移植協(xié)會(huì)年會(huì)上,初次公布了動(dòng)物實(shí)驗(yàn)的初步成果,該科學(xué)家的名字從此被國(guó)際移植醫(yī)學(xué)界所熟知。
研究人員通過(guò)一系列臨床前動(dòng)物實(shí)驗(yàn)研究發(fā)現(xiàn)了炎*轉(zhuǎn)化調(diào)控網(wǎng)絡(luò)的關(guān)鍵節(jié)點(diǎn),加上跨學(xué)科的交叉對(duì)這些關(guān)鍵節(jié)點(diǎn)進(jìn)行靶向藥物的設(shè)計(jì),然后再做臨床研究,進(jìn)行臨床療效的驗(yàn)證和在臨床的轉(zhuǎn)化應(yīng)用。老藥***結(jié)腸*新用處的發(fā)現(xiàn)便是一個(gè)典型案例。過(guò)去研究證明,炎癥性腸病是誘發(fā)結(jié)腸*的主要因素之一,但炎*轉(zhuǎn)化的分子機(jī)制尚不明了。圍繞這個(gè)問(wèn)題,基礎(chǔ)研究者發(fā)現(xiàn)了調(diào)控炎癥與**的關(guān)鍵性節(jié)點(diǎn)。隨后,臨床研究者接過(guò)接力棒,用臨床前動(dòng)物實(shí)驗(yàn)的實(shí)驗(yàn)動(dòng)物模型驗(yàn)證了這一關(guān)鍵性節(jié)點(diǎn)的作用。化妝品臨床前動(dòng)物實(shí)驗(yàn)包括哪些?

下面提供了關(guān)于臨床前動(dòng)物實(shí)驗(yàn)研究監(jiān)測(cè)的具體建議:(1)術(shù)中監(jiān)測(cè):術(shù)中和術(shù)后對(duì)心率、心電圖、血壓和血?dú)獾谋O(jiān)測(cè)有助于獲得積極結(jié)果。(2)急性(短期)研究:建議**記錄生命體征,如手術(shù)時(shí)記錄的心律、呼吸頻率、脈搏和血壓。這些信息應(yīng)與植入、放置或使用裝置、造影劑或其他裝置相關(guān)材料的時(shí)間相關(guān)聯(lián),并在麻醉和手術(shù)記錄中注明。(3)慢性(長(zhǎng)期)研究:慢性研究包括如下不同時(shí)期:①術(shù)后護(hù)理:建議遵循目前的實(shí)驗(yàn)室實(shí)驗(yàn)動(dòng)物護(hù)理標(biāo)準(zhǔn),保持動(dòng)物體溫正常,盡量減少疼痛和***,并提供充足的液體和電解質(zhì)。獲取動(dòng)物生理信息的質(zhì)量應(yīng)與人類(lèi)護(hù)理和康復(fù)中所獲得的信息相類(lèi)似。此外,還應(yīng)建立一個(gè)標(biāo)準(zhǔn)評(píng)估模式來(lái)控制壓力變量,以監(jiān)測(cè)疼痛和體溫,并根據(jù)中期結(jié)果指導(dǎo)額外的保溫和止痛藥使用。中成藥臨床前動(dòng)物實(shí)驗(yàn)多少錢(qián)?云南個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)外包
中成藥臨床前動(dòng)物實(shí)驗(yàn)價(jià)格;吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
在數(shù)據(jù)分析與結(jié)果解讀方面,實(shí)驗(yàn)數(shù)據(jù)需經(jīng)過(guò)統(tǒng)計(jì)分析,評(píng)估實(shí)驗(yàn)結(jié)果的可靠性和統(tǒng)計(jì)學(xué)差異。同時(shí),對(duì)實(shí)驗(yàn)結(jié)果的可行性和適用性進(jìn)行評(píng)估,為臨床試驗(yàn)提供科學(xué)依據(jù)。此外,倫理和安全考慮也是臨床前動(dòng)物實(shí)驗(yàn)不可忽視的方面。實(shí)驗(yàn)過(guò)程應(yīng)嚴(yán)格遵守倫理和安全規(guī)范,確保實(shí)驗(yàn)動(dòng)物得到合理的動(dòng)物福利,并盡量減少實(shí)驗(yàn)本身以外的變量,以保證實(shí)驗(yàn)結(jié)果的可靠性。臨床前動(dòng)物實(shí)驗(yàn)的具體內(nèi)容和要求還可能受到藥物類(lèi)型、研究目的、法規(guī)要求等多種因素的影響,因此在實(shí)際操作中,還需根據(jù)具體情況進(jìn)行調(diào)整和優(yōu)化。綜上所述,臨床前動(dòng)物實(shí)驗(yàn)的具體內(nèi)容和要求涵蓋了實(shí)驗(yàn)?zāi)康摹?dòng)物選擇、實(shí)驗(yàn)操作、數(shù)據(jù)分析與結(jié)果解讀以及倫理和安全考慮等多個(gè)方面,這些步驟和要求的嚴(yán)格執(zhí)行對(duì)于確保實(shí)驗(yàn)結(jié)果的準(zhǔn)確性和可靠性具有重要意義。吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
擴(kuò)展資料
臨床前動(dòng)物實(shí)驗(yàn)熱門(mén)關(guān)鍵詞
臨床前動(dòng)物實(shí)驗(yàn)企業(yè)商機(jī)
- . 陜西有什么臨床前動(dòng)物實(shí)驗(yàn)外包
- . 甘肅靠譜臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?
- . 云南值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)
- . 內(nèi)蒙古比較好的臨床前動(dòng)物實(shí)驗(yàn)外包
- . 陜西個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 江西值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
- . 云南個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)公司
- . 專(zhuān)業(yè)臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)
- . 貴州高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)是什么
- . 廣東專(zhuān)業(yè)臨床前動(dòng)物實(shí)驗(yàn)指標(biāo)
臨床前動(dòng)物實(shí)驗(yàn)行業(yè)新聞
- . 河北什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 河南值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)研究
- . 生物藥臨床前動(dòng)物實(shí)驗(yàn)是什么
- . 化妝品臨床前動(dòng)物實(shí)驗(yàn)指導(dǎo)原則
- . 黑龍江個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)外包
- . 吉林什么是臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 西藏有什么臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
- . 靠譜臨床前動(dòng)物實(shí)驗(yàn)外包
- . 云南有什么臨床前動(dòng)物實(shí)驗(yàn)是什么
- . 寧夏靠譜臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?
-
云南個(gè)性化臨床前動(dòng)物實(shí)驗(yàn)是什么
-
四川值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)研究
-
內(nèi)蒙古有什么臨床前動(dòng)物實(shí)驗(yàn)外包
-
浙江高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
-
江蘇值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)價(jià)格
-
黑龍江值得信賴(lài)臨床前動(dòng)物實(shí)驗(yàn)
-
陜西有什么臨床前動(dòng)物實(shí)驗(yàn)評(píng)價(jià)
-
湖北臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)
-
黑龍江高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)多少錢(qián)
-
江蘇臨床前動(dòng)物實(shí)驗(yàn)研究