商機詳情 -
上海原位雜交哪家靠譜
組織芯片技術誕生于 20 世紀 90 年代末,較初旨在解決傳統病理學研究中樣本量大、檢測效率低的問題。從手工制作的簡易芯片雛形,逐步發展到如今高度自動化、標準化的制作流程,其技術不斷革新。早期,樣本的獲取和固定方式較為粗糙,隨著技術進步,采用了更精細的微切割技術和優化的固定液配方,確保了組織樣本的完整性和生物活性。這一發展歷程使得組織芯片能夠容納更多的樣本,并且在檢測的準確性和重復性上有了質的飛躍,為大規模的醫學研究提供了有力支持。多種位點組織芯片應用通過創新的樣本布局設計,在同一張芯片上實現對多個組織位點的集中檢測。上海原位雜交哪家靠譜
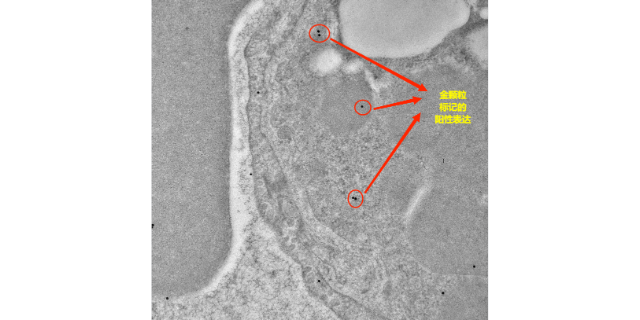
組織芯片技術是將大量不同來源的組織樣本,按照特定的陣列方式排列在一張載玻片上。其重心原理是借助精密的組織陣列儀,從供體組織塊中獲取直徑通常為 0.6 - 2mm 的微小組織芯,然后將這些組織芯有序地移植到受體蠟塊中。制成的組織芯片在后續實驗中,可同時對多個樣本進行同一指標的檢測,如免疫組化、原位雜交等。通過一次實驗,就能獲得大量組織樣本的信息,較大提高了研究效率,組織芯片技術為大規模的組織學研究提供了高效的技術平臺。寧波多種位點組織芯片多重免疫熒光平臺憑借其獨特的酪胺信號放大(TSA)技術,展現出明顯的多重檢測與高靈敏度優勢。
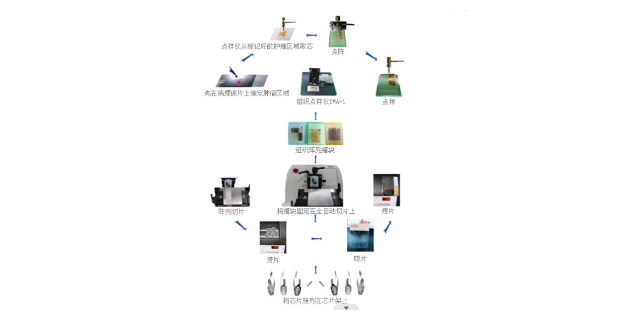
原位雜交技術服務適用于多種樣本類型,在基礎科研與臨床應用中展現出良好的兼容性。對于石蠟包埋組織切片,通過脫蠟、水化和抗原修復等預處理步驟,可有效去除石蠟干擾,恢復核酸可及性;新鮮冰凍組織樣本需在低溫條件下切片并及時固定,防止核酸降解與組織結構破壞。細胞樣本無論是培養細胞系還是原代細胞,均可通過涂片、爬片或細胞塊制作等方式進行處理。此外,特殊樣本如古生物化石、環境微生物群落樣本等,也能通過優化實驗條件實現檢測。這種廣闊的樣本適應性,使原位雜交技術能夠滿足不同研究場景需求,從病理組織的基因異常分析到環境樣本的微生物基因檢測,均可發揮重要作用。
多種位點組織芯片產生的數據豐富且復雜,需要采用深度系統的分析方法進行解讀。在數據處理過程中,借助專業的圖像分析軟件,對芯片上每個位點的染色結果進行數字化處理,精確提取目標蛋白表達強度、陽性細胞比例等量化指標。通過統計學方法,對不同位點間的數據進行對比分析,挖掘組織樣本中的共性與差異特征。此外,結合生物信息學技術,將芯片數據與基因表達譜、臨床信息等多維度數據進行整合分析,構建復雜的生物網絡模型,揭示組織樣本中分子間的相互作用關系。這種深度系統的數據分析方式,能夠從海量數據中提煉出有價值的生物學信息,為疾病機制研究、預后評估以及藥物靶點發現等提供有力的數據支持,提升研究成果的科學性和實用性。多重免疫熒光平臺具有明顯的信號放大和多輪染色特點,為其在復雜生物樣本分析中提供了獨特的優勢。
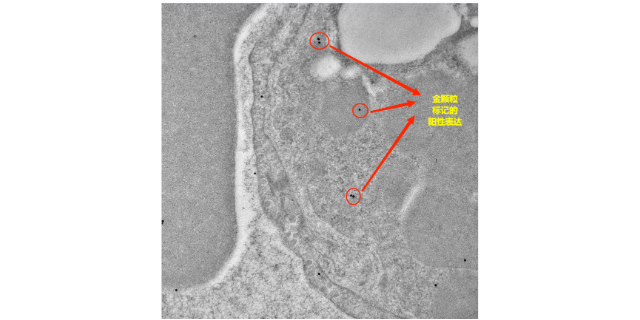
隨著生命科學和醫學研究的不斷深入,組織芯片技術的市場前景十分廣闊。在科研領域,各大高校、科研機構對組織芯片的需求持續增長,用于基礎研究、藥物研發等項目。在臨床診斷方面,組織芯片可作為輔助診斷工具,幫助醫生更準確地判斷疾病類型和預后,未來有望在臨床廣泛應用。在制藥企業中,組織芯片技術可加速藥物研發進程,降低研發成本,市場需求巨大。隨著技術的不斷推廣和應用,相關的技術服務市場也將不斷擴大,包括芯片制作、實驗檢測、數據分析等一站式服務,預計未來幾年組織芯片技術市場將保持穩定增長態勢。多種位點組織芯片應用在生命科學領域有著廣闊多元的應用場景。組織芯片免疫熒光服務
組織芯片免疫熒光方案的重點功能在于其高通量檢測能力和數據整合能力。上海原位雜交哪家靠譜
原位雜交解決方案以核酸堿基互補配對為基礎,實現特定核酸序列在細胞或組織中的可視化定位。該方案通過設計與目標核酸互補的探針,經標記處理后與樣本中的核酸進行雜交反應。常用的標記物如熒光素、地高辛等,賦予探針可檢測的信號特征。在雜交過程中,嚴謹控制溫度、離子強度等條件,確保探針與目標核酸特異性結合,避免非特異性雜交干擾。反應完成后,通過顯色或熒光檢測技術,將目標核酸的分布與豐度直觀呈現。相較于其他核酸檢測方法,原位雜交能夠保留樣本的組織結構完整性,在細胞層面實現核酸的精確定位,為研究基因表達模式、病毒染病位點等提供獨特視角,助力探索生命過程中的分子機制。上海原位雜交哪家靠譜