商機詳情 -
廈門正規外泌體提取試劑供應商
外泌體的提取、分離方法:開發高效、快速、穩定,并且保持外泌體結構和生物功能完整性的方法,是目前外泌體應用于臨床的基礎和前提。從細胞上清和體液中提取分離外泌體的方法很多,但是外泌體的純度和產量卻和分離方法息息相關。通常分離步驟少、產率高,但是純度會受到影響。鑒于每種分離方法都有其優缺點,實驗可以根據樣本來源、下游實驗目的等,選擇合適的外泌體分離方法。2015年,國際囊泡組織(InternationSocietyforExtracelluarVesicles,ISEV)指出,簡單依靠一種分離方法得到的外泌體的純度和產量都難滿足實驗的需求。因此,推薦聯合使用各種方法,從而得到高純度和高產量的外泌體。外泌體提純試劑盒的特色與優勢:無需耗時的超速離心,過濾或特殊注射器。廈門正規外泌體提取試劑供應商
外泌體的提取、分離方法:微流控技術。微流控是利用微納米級尺寸的管道來處理和操控流體所涉及的一門技術,其在外泌體分離方面的應用受到越來越多學者的關注。Jie等[16]課題組開發了一種三維納米結構微流控芯片,微柱陣列通過化學沉積將交叉多壁碳納米管功能化,然后其就可以識別特定的分子(CD63)并利用獨特拓撲納米材料高效的捕獲外泌體。Wunsch等[17]利用硅工藝生產納米級確定性側向位移(Nano-DLD)芯片,得到了均勻的間隙尺寸,該芯片可以靈敏地將20~110nm的顆粒分離。該研究證明了外泌體基于大小的位移,從而揭示了利用芯片分選和量化納米級生物膠體的潛力。長沙正規外泌體提取試劑哪家好外泌體的提取方法學規范、統一定量及鑒定等。

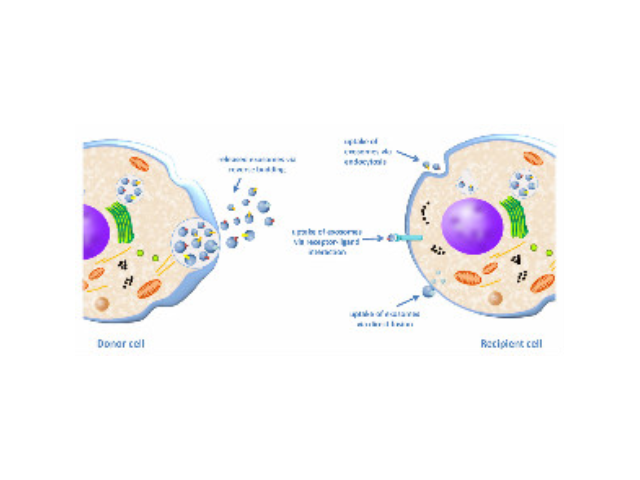
外泌體(exosomes)是活細胞經過"內吞-融合-外排"等一系列調控過程而形成的膜性囊泡,來源于晚期核內體(也稱為多囊泡體),直徑約為30-150nm,密度在1.13-1.21g/ml,天然存在于血液、唾液、尿液及母乳等體液中,同時外泌體也存在于組織和細胞間隙中。人體中幾乎所有類型的細胞均能產生外泌體,人體中大約有1014個外泌體,大約平均每個細胞產生1000-10000個。外泌體中含有核酸(DNA、miRNA、lncRNA、mRNA、tRF等)、蛋白和脂類,在細胞間物質和信息轉導中發揮重要作用,研究表明其在干細胞、免疫調控、瘤轉移、血管生成以及生物標志物等領域都發揮著不可替代的作用
由于外泌體的特殊結構和功能,使得它具有潛在的應用價值,一方面可以作為診斷多種疾病的生物指標,另一方面也可以作為治病手段,未來有可能作為藥物的天然載體用于臨床治病。外泌體的分離純化一直是科研工作者關注的問題,獲得高純度的外泌體對后續的研究至關重要。據了解,目前人們多采用超速離心、免疫磁珠、超濾、沉淀或試劑盒等方法實現外泌體的提取分離。外泌體攜帶大量特異性的蛋白質(如細胞因子、生長因子)以及功能性的mRNAs、miRNAs等生物活性物質,在體內參與細胞通訊、細胞遷移、促血管新生和抗一些病癥免疫等生理過程,與多種疾病的發生和進程密切相關。外泌體提取:根據外泌體的大小,從蛋白質和其他大分子中分離外泌體。

外泌體與神經退行性疾病:外泌體可能促進或限制大腦中未折疊和異常折疊的蛋白質的聚集。AD病人腦脊液外泌體中均可檢測到Tau和Aβ蛋白。類似的現象也在PD和ALS疾病中發現。PD病人腦脊液外泌體可檢測到α-synuclein,ALS病人外泌體中也可以檢測到SOD1或TDP-43。外泌體與疾病診斷(應用潛能):外泌體生成機制表明,通過分析外泌體的組分,可以幫助識別其來源的細胞類型。這一特性已被應用于開發心血管疾病,神經系統疾病和一些病癥的分子診斷方法,也在肝腎肺相關疾病中進行研發測試。將沉淀物用PBS緩沖液進行懸浮,使外泌體懸浮于液體上層外泌體提純試劑盒的特色與優勢:適用于多種物種。溫州外泌體提取試劑廠家
外泌體提取色譜法是利用根據凝膠孔隙的孔徑大小與樣品分子尺寸的相對關系而對溶質進行分離的分析的方法。廈門正規外泌體提取試劑供應商
外泌體的提取方法:1.超速離心法(差速離心)。超離法是較常用的外泌體純化手段,采用低速離心、高速離心交替進行,可分離到大小相近的囊泡顆粒。超離法因操作簡單,獲得的囊泡數量較多而廣受歡迎,但過程比較費時,且回收率不穩定(可能與轉子類型有關),純度也受到質疑;此外,重復離心操作還有可能對囊泡造成損害,從而降低其質量。2.密度梯度離心。在超速離心力作用下,使蔗糖溶液形成從低到高連續分布的密度階層,是一種區帶分離法。通過密度梯度離心,樣品中的外泌體將在1.13-1.19g/ml的密度范圍富集。此法獲得的外泌體純度較高,但步驟繁瑣,耗時,對離心時間極為敏感廈門正規外泌體提取試劑供應商