商機詳情 -
遼寧專業的eae模型實驗外包
從鳥類到哺乳類的多種動物如雞、小鼠、大鼠、豚鼠、家兔、羊、犬、猴等均可成功誘發EAE,但不同種屬或同一種屬不同品系動物的敏感性有很大差異。對EAE敏感的動物有Lewis、DA大鼠,PL/J、SJL/J小鼠,Hartley、Strain13豚鼠。雖然豚鼠對誘發EAE相當敏感,但其品系復雜,有關試劑缺乏,一般不常用作實驗對象。相比之下大鼠及小鼠的背景知識及相關試劑則較為普遍,遺傳學、免疫學等方面的研究也較深入,且其EAE在臨床、病理、免疫及生化改變等方面都與人類脫髓鞘疾病較為相似,因此應用比較為普遍。EAE模型是由針對CNS髓鞘發生免疫攻擊的CD4+Th1細胞介導的自身免疫性疾病。遼寧專業的eae模型實驗外包
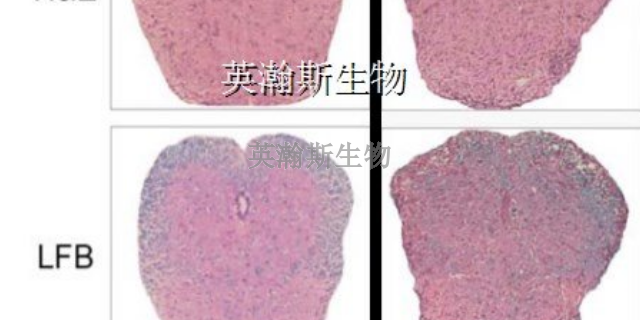
MOG,英文全名Myelinoligodendrocyteglycoprotein,中文名髓鞘少突膠質細胞糖蛋白,髓鞘的一種微量成分,屬于免疫球蛋白超家族成員之一。t也是特定表達于***系統(CNS)的自身抗原,誘導多發性硬化癥的原發性脫鞘特征。MOG(35-55)是髓鞘少突膠質細胞糖蛋白的免疫優勢表位,能夠誘導強烈的T細胞和B細胞應激反應,具高度致腦炎性,能夠誘導嚙齒類動物的實驗性白身免疫性腦脊髓炎(EAE)模型。EAE是**普遍的MS動物模型,具有MS許多的臨床和病理生理學特征。單次注射MOG(35-55)能夠產生一種復發-緩解型神經性疾病,表現出大量斑塊狀脫髓鞘病癥。1-甲基-4-苯基-1,.2,3,6-四氫吡啶(MPTP)誘導的多巴胺神經元損傷模型,免疫接種MOG(35-55)能抑制該神經元的白發再生功能。寧夏靠譜的eae模型如何構建EAE小鼠模型可以反映MS的很多臨床特征。
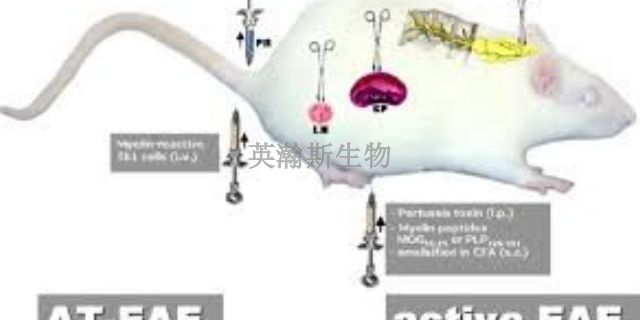
獲取實驗性自身免疫性腦脊髓炎(EAE)模型小鼠小膠質細胞,并檢測其特性。方法取8周齡,雌性C57BL/6小鼠行EAE造模,待至發病高峰期(第15天)時以PBS灌注后取小鼠后腦和脊髓,切碎后加胰酶消化,消化完成后通過100μm濾網濾過,而后采用Percoll密度梯度離心法分離獲取單個核細胞,進一步利用CD11b與CD45抗體染色,通過流式細胞儀分選CD11b~+CD45~(high)和CD11b~+CD45~(low)細胞,即分別得到相對活化和靜息的小膠質細胞,***對流式分選獲取的小膠質細胞行qPCR檢測。結果通過形態比較,獲得了高純度的小膠質細胞。FIZZ-1基因行qPCR檢測,結果顯示在EAE急性期M2型小膠質細胞明顯增多,符合文獻報道。結論該方法能從EAE小鼠體內分離獲取高純度的小膠質細胞,可用于相關目的基因后續檢測。
利用EAE動物模型,科學家們得以深入研究多發性硬化癥(MS)對大腦認知功能的影響及其潛在干預手段。這一模型能夠模擬MS患者大腦神經系統的病理變化,包括神經纖維的脫髓鞘、神經元損傷以及炎癥反應等,從而為我們提供了一個獨特的實驗平臺。通過觀察EAE動物模型在認知任務中的表現,科學家們能夠評估MS對大腦認知功能的損害程度,并探究其背后的神經生物學機制。同時,利用這一模型,科學家們還可以測試不同的干預手段,如藥物療愈、康復訓練等,以評估它們對改善認知功能的效果。因此,利用EAE動物模型深入研究MS對大腦認知功能的影響及其潛在干預手段,對于推動MS的臨床療愈和研究具有重要意義。AE模型已經直接幫助了三種藥物的開發。
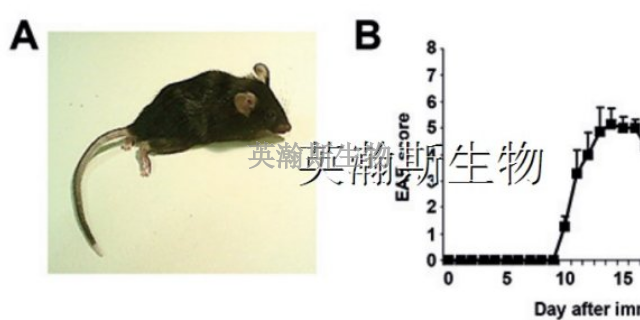
EAE動物模型的建立為多發性硬化癥(MS)的臨床研究提供了不可或缺的動物實驗基礎。這一模型不僅模擬了MS在人體內的病理過程,還使得科學家們能夠在控制實驗條件的情況下,對疾病的發生、發展以及***反應進行深入研究。通過觀察和記錄EAE動物模型在疾病進程中的表現,科學家們能夠收集到大量有價值的實驗數據,為MS的發病機制、病理變化以及***效果的評估提供重要依據。此外,EAE動物模型還為新藥物的研發和現有***方法的優化提供了實驗平臺,使得科學家們能夠在動物體內測試藥物的有效性和安全性,為MS的臨床***提供更加可靠的依據。因此,EAE動物模型的建立對于推動MS的臨床研究具有重要意義。EAE模型小鼠中致炎細胞Th17數量增加,抑炎細胞Treg和Breg數量降低。上海哪里有eae模型實驗外包
MOG是目前常用建立EAE模型的髓鞘抗原,多以誘發慢性EAE(Chronic EAE)模型。遼寧專業的eae模型實驗外包
不同品種或同一品種不同品系動物對EAE模型的易感性主要受免疫反應基因(Ir基因)影響,Ir基因的調節作用表現為T細胞表面受體對髓鞘堿性蛋白(MBP)的特異性表達。動物的種類不同,其受體表達能力不同,對自身抗原的反應性不同,因而對EAE的易感性也不同,因此在選擇動物時需要尋找EAE模型的敏感動物。鑒于對EAE模型敏感的Lewis、DA大鼠,PL/J,SJL/J小鼠的價格更加昂貴、不宜獲得且難以飼養,國內多采用價廉易得的Wistar大鼠,但其敏感性不及前者。遼寧專業的eae模型實驗外包